اسید فرمیک (کاربردها و بازار جهانی)

در این مقاله به سراغ اسید فرمیک رفته ایم و می خواهیم بدانیم که اسیدفرمیک چیست، در مورد تاریخچه این ماده شیمیایی بیشتر بدانیم ، بدانیم چگونه تولید می شود، در چه صنایعی استفاده می شود و همین طور به بررسی بازار جهانی این ماده شیمیایی بپردازم:
اسیدفرمیک چیست؟
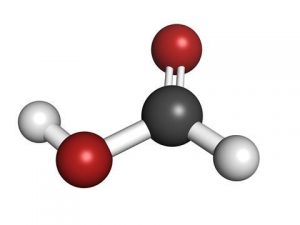
فرمول شیمیایی اسید فرمیک HCOOH است و یک مولکول مسطح است.
اسیدفرمیک یک مایع بی رنگ و دودزا است که با آب مخلوط می شود. در مرحله بخار ، بیشتر از مولکول های جداگانه از دیمرهای پیوند خورده با هیدروژن تشکیل شده است. در مرحله گاز، انحراف قابل توجهی از قانون گاز ایده آل در نتیجه این پیوند هیدروژنی بوجود می آید. در حالت مایع و جامد، اسید فرمیک را می توان به عنوان یک شبکه بی نهایت مولکول های پیوند یافته با هیدروژن تصور کرد.
اسید فرمیک که در سری کربوکسیلیک اسید اولین است. بیشتر خواص شیمیایی مشابهی دارد و بنابراین با قلیاها واکنش داده. و نمک های فرمت محلول در آب را تشکیل می دهد. اما اسید فرمیک در بین اسیدهای کربوکسیلیک منحصر به فرد است زیرا با آلکن ها واکنش داده و استرهای فرمی را تشکیل می دهد. در حضور اسیدهای سولفوریک و هیدروفلوئوریک ، یک نوع واکنش گاترمن-کوچ رخ می دهد. و اسید فرمیک به آلکن می افزاید تا اسید کربوکسیلیک بزرگتری تولید کند.
تاریخچه اسیدفرمیک:
بیش از 600 سال طبیعت شناسان می دانستند. که تپه های مورچه ها بخار اسیدی تولید می کنند. در سال 1671، جان ری، طبیعت شناس انگلیسی، جداسازی ماده فعال را توصیف کرد. برای انجام این کار او تعداد زیادی مورچه مرده را جمع آوری و تقطیر کرد. و اسیدی که بعداً کشف کرد از کلمه لاتین به معنی مورچه ، فرمیکا به اسید فرمیک معروف شد. نام مناسب آن IUPAC اکنون متانوئیک اسید است.
اولین سنتز اسید فرمیک توسط شیمی دان فرانسوی ژوزف گی لوساک انجام شد. که از اسید هیدروسیانیک به عنوان ماده اولیه استفاده کرد. در سال 1855 ، یکی دیگر از شیمیدانان فرانسوی ، مارسلین برتلوت ، یک سنتز از مونوکسید کربن ایجاد کرد. که مشابه آنچه امروزه استفاده می شود.
اسید فرمیک نیز در حالت طبیعی در گزنه ها وجود دارد. و مسئول احساس سوزش در تماس با آن ها است. همچنین در نیش و نیش حشرات بسیاری از جمله زنبورها و مورچه ها یافت می شود. که از آن به عنوان مکانیسم دفاعی شیمیایی استفاده می کنند. هنگامی که مورچه غده سمی خود را منقبض می کند. اسید فرمیک ذخیره شده در این غده در گزش عبور می کند و با جت ها (در برخی از گونه ها تا فاصله یک متر) به طرف مهاجمان مورچه منتقل می شود. از آنجا که pH اسید فرمیک 2-3 پوند است. مهاجمان معمولاً فرار می کنند، یا کشته می شوند.
تولید:
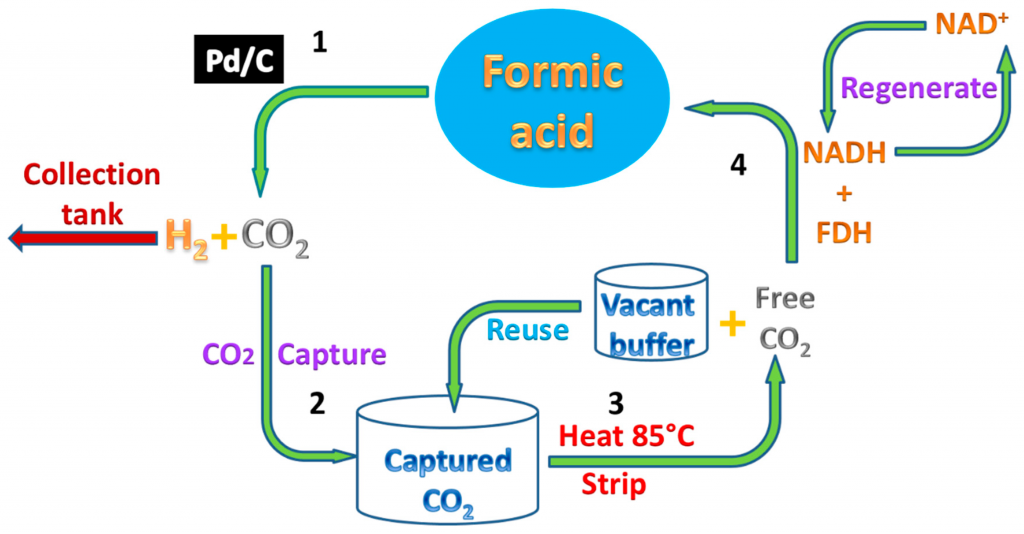
اسید فرمیک به عنوان یک محصول جانبی در تولید اسید استیک تولید می شود. با این حال ، تقاضای صنعتی برای اسید فرمیک بیشتر از آن چیزی است که می توان از این مسیر تهیه کرد ، بنابراین مسیرهای تولید اختصاصی ایجاد شده است. بر اساس معادله شیمیایی ، یک روش متانول و مونوکسید کربن را در حضور یک پایه قوی مانند متوکسید سدیم ترکیب می کند تا متیل فرمت تولید شود.
کاربرد:
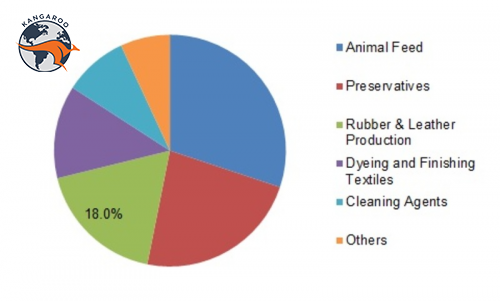
کاربرد اصلی این ماده شیمیایی به شرح ذیل می باشد:
- خوراک دام در اروپا ، به عنوان عامل نگهدارنده و ضد باکتری است. می توان روی یونجه تازه یا سایر سیلوها سمپاشی کرد تا برخی فرایندهای پوسیدگی متوقف یا به تأخیر بیفتد. بنابراین اجازه می دهد تا خوراک بیشتر زنده بماند. و بنابراین به طور گسترده ای برای حفظ غذای زمستانی برای گاو استفاده می شود.
- در صنعت طیور ، گاهی اوقات برای از بین بردن باکتری سالمونلا به خوراک اضافه می شود.
- برخی از زنبورداران نیز از اسید فرمیک به عنوان دود کننده برای کشتن کنه ای که به زنبورها حمله می کند ، استفاده می کنند.
- اسید فرمیک در رنگرزی و تکمیل منسوجات،
- برنزه کردن چرم ،
- حمام آبکاری نیکل ،
- آبکاری ،
- لاتکس لاستیکی منعقد کننده ،
- بازسازی لاستیک قدیمی
- در برخی از رنگ کننده های تجاری استفاده می شود.
- از آن برای ساختن نمک های فلزی شامل نیکل ، کادمیوم و فرمات پتاسیم استفاده می شود.
- به عنوان حلال برای عطرها و در ساخت لاک ، شیشه ، پلاستیک کننده های رزین وینیل و استرهای فرمت برای طعم و عطر استفاده می شود.
- از آن در سنتز شیرین کننده مصنوعی ، آسپارتام استفاده می شود.
بازار جهانی:
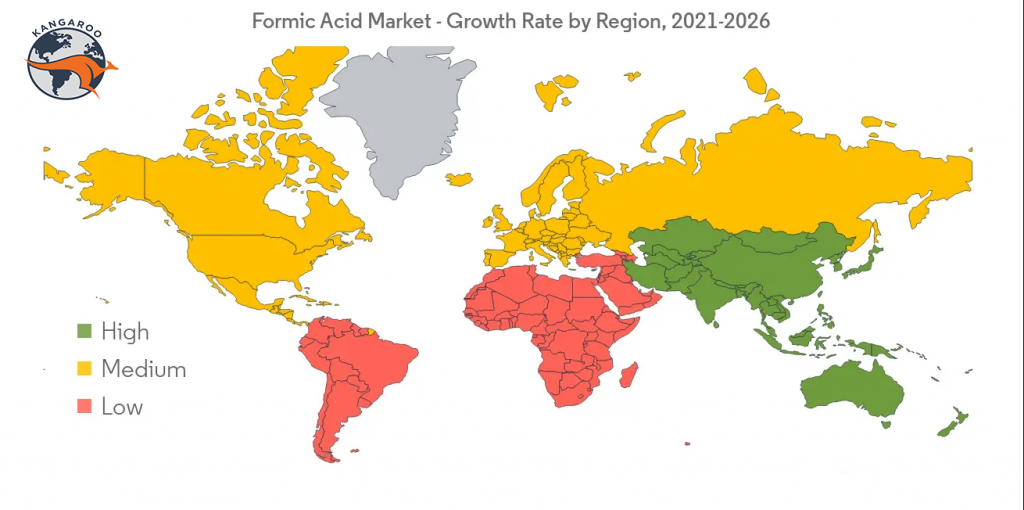
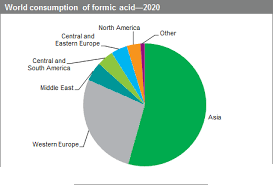
شرکت علمی سازان پاسارگاد با برند کانگورو، تامین کننده مواد اولیه شیمیایی می باشد. جهت خرید اسید فرمیک با شماره 88064800 تماس حاصل نمائید. همکاران ما آماده ارائه مشاوره و ثبت سفارشات شما می باشند
نگارنده: مهناز معصومی راد
منبع: http://www.chm.bris.ac.uk




















